Mise à jour : Mai 2023
L'épidémie de COVID-19 est déclarée par l'OMS le 9 janvier 2020. Les connaissances de cette maladie ont évolué et des nouvelles recommandations sont mis à jour régulièrement.
Nous vous proposons de lire les nouveaux articles sur ce sujet :
- Nouvelles recommandations vaccinales contre la covid 19 pour l'année 2023 (mes vaccins.net)
- Vaccination et Covid-19, trois ans plus tard (Vidal actualités)
![]() AI-JE BESOIN D'UNE 4ème DOSE DE VACCIN COVID ?
AI-JE BESOIN D'UNE 4ème DOSE DE VACCIN COVID ?
L’épidémie de Covid-19 a fortement décru depuis le début du mois de février 2022, elle semble aujourd’hui stagner voire repartir à la hausse, notamment avec la propagation de BA.2, nouveau sous-variant d’Omicron.
Les bénéfices immunologiques apportés par la vaccination de rappel (c'est-à-dire «3e dose») contre SARS-CoV-2 tendent à diminuer rapidement chez les seniors, les autorités sanitaires de divers pays se sont prononcées pour l'administration d'un 2e rappel (c'est-à-dire «4e dose») chez les personnes âgées.
Ce rappel est recommandé par plusieurs pays pour les sujets âgés et ayant comorbidités mais il n’y a pas de consensus sur le délai entre la 3e et la 4e dose.
- En France, il s'agit des personnes de plus de 80 ans, de celles de plus de 65 ans qui présentent des facteurs de risque de forme grave, et des personnes âgées vivant en institution.
- Aux États-Unis, la Food and Drug Administration (FDA) a autorisé une 2e dose de rappel chez les personnes de 50 ans et plus, au moins 4 mois après le 1er rappel, en prévision de la vague de variant BA.2 qui est sur le point d'arriver dans ce pays;
- En Allemagne, la 2e dose de rappel est proposée aux 70 ans et plus, ainsi qu'aux personnes immunodéprimées ou résidant en EHPAD (établissement d'hébergement pour personnes âgées dépendantes), au moins 3 mois après le 1er rappel;
- En Suède, elle est proposée aux personnes de plus de 80 ans, celles en EHPAD ou hospitalisées au domicile, au moins 1 mois après le 1er rappel.
PRÉCAUTIONS COMMUNES À TOUTE VACCINATION :
Il n’existe aucune donnée sur l'interchangeabilité entre les différents vaccins. Pour compléter le schéma de vaccination, les individus ayant reçu une première dose doivent recevoir une deuxième injection du même vaccin afin que le schéma de vaccination soit complet.
![]() POPULATION PÉDIATRIQUE :
POPULATION PÉDIATRIQUE :
Les vaccins sont indiqués aux personnes âgées de plus de 18 ans sauf les suivants :
- l'EMA européen a approuvé le vaccin Pfizer/BioNTech (COMIRNATY®) pour les 12-15 ans. Une autorisation des deux parents est obligatoire. La présence d'au moins un parent est indispensable lors de la vaccination.
- La tolérance et l’efficacité sont à l'étude. Pfizer (COMIRNATY®) et Moderna (SPIKEVAX®) ont publié les résultats des études montrant que leurs vaccins sont "efficaces" pour les jeunes à partir de 12 ans.
![]() GROSSESSE ET ALLAITEMENT :
GROSSESSE ET ALLAITEMENT :
VACCIN À ARNm :
Les vaccins à ARNm contre la Covid-19 ne sont pas tératogènes ni foetotoxiques chez l’animal.
Depuis le début de la vaccination contre la Covid-19 par les vaccins à ARNm aux USA, les femmes enceintes qui le souhaitent peuvent être vaccinées, quel que soit le terme de leur grossesse.
Vaccin à vecteur viral :
Les études de toxicité sur la reproduction chez l’animal sont en cours. Sur la base des résultats d’une étude préliminaire, aucun effet nocif n’est attendu sur le développement foetal. Les données concernant d’éventuelles grossesses exposées lors des essais cliniques ne sont pas disponibles à ce jour.
La vaccination contre la Covid-19 est possible en cours de grossesse. Compte tenu des données disponibles, on préférera un vaccin à ARNm
Si possible, débuter le protocole entre 10 et 20 semaines d’aménorrhée, c’est-à-dire après la fin de l’organogenèse et suffisamment tôt pour que la femme enceinte soit protégée au 3ème trimestre.
ALLAITEMENT : Le passage systémique de l’ARNm et du vecteur viral après la vaccination n’étant pas attendu, leur présence dans le lait ne l’est pas non plus.
Les vaccins à ARNm et à vecteur viral contre la Covid-19 sont dépourvus de pouvoir infectant. L’enfant allaité ne risque donc pas d’être infecté par le vaccin effectué à sa mère.
Source : Centre de Référence sur les Agents Tératogènes crat.fr
![]() VACCINATION DES PATIENTS DÉJÀ INFECTÉS PAR LE COVID :
VACCINATION DES PATIENTS DÉJÀ INFECTÉS PAR LE COVID :
Attendre un délai de 3 à 6 mois après la guérison et de préférence 6 mois. Une seule dose de vaccin est conseillée (HAS-santé.fr février 2021).
Deux exceptions :
- les personnes présentant une immunodépression avérée (en particulier celles qui reçoivent un traitement immunosuppresseur) doivent, après un délai de 3 mois après le début de l’infection par le SARS-CoV-2, être vaccinées par le schéma à deux doses,
- les personnes qui ont reçu une première dose de vaccin et qui présentent une infection par le SARS-CoV-2 avec PCR positive dans les jours qui suivent cette première vaccination ne doivent pas recevoir la seconde dose dans les délais habituels, mais dans un délai de 3 à 6 mois après l’infection.
- La réalisation d’une sérologie pré-vaccinale n’est pas pertinente et donc non recommandée,
- La présence de symptômes persistants après une Covid-19 n’est pas une contre-indication à la vaccination. Toutefois dans ce cas, une consultation médicale adaptée est nécessaire avant la vaccination pour juger au cas par cas de l’intérêt de celle-ci (HAS-santé-fr).
![]() QUELS SONT LES SIGNES EN CAS D'ALLERGIE ?
QUELS SONT LES SIGNES EN CAS D'ALLERGIE ?
Le risque allergique existe avec tous les vaccins ou à l'un de leurs excipients mais ce risque est rare.
Les vaccins Moderna, BioNTech et de Pfizer, à ARN messager, contiennent des Macrogols (polyéthylène glycol) [tous les laxatifs comparables aux FORLAX, ILAX, TRANSITON, OSMOLAX, MOVICOL, MICROLAX].
La réaction allergique apparaît en moins d'une heure, elle peut être instantanée. Le patient doit être surveillé au moins 30 minutes après l'injection.
- Les éruptions généralisées (urticaire).
- L'apparition d'une gêne respiratoire (bronchospasme),
- Le choc anaphylactique.
Hypersensibilité et anaphylaxie : adrénaline dans les formes sévères, hospitalisation pour surveillance même si les symptômes régressent rapidement. Il convient de toujours disposer d’un traitement médical approprié et de surveiller le sujet vacciné en cas de survenue d’une réaction anaphylactique suite à l’administration du vaccin. Les formes bénignes répondent aux antihistaminiques.
Réactions liées à l'anxiété : des réactions liées à l'anxiété, dont des réactions vasovagales (syncope), une hyperventilation ou des réactions liées au stress peuvent survenir lors de la vaccination reflétant une réaction psychogène à l'injection via l’aiguille. Il est important que des précautions soient prises pour éviter toute blessure en cas d'évanouissement.
Plus de détails : Voir nos articles
![]() VACCINS COVID-19 ET EFFETS THROMBOTIQUES (recommandations ANSM 12/5/2021) :
VACCINS COVID-19 ET EFFETS THROMBOTIQUES (recommandations ANSM 12/5/2021) :
Toute personne présentant des symptômes neurologiques, notamment des maux de tête sévères ou persistants ou une vision floue après la vaccination, ou présentant des ecchymoses (pétéchies) à distance du site d'injection quelques jours après la vaccination, doit rapidement consulter un médecin.
Les professionnels de santé doivent être attentifs aux signes et symptômes évocateurs de thrombose associée ou non à une thrombopénie chez les personnes vaccinées par les vaccins Vaxzevria (AstraZeneca) et Janssen afin de réaliser les examens biologiques et d’imagerie adéquats pour une prise en charge la plus précoce possible de ces patients.
Ces thromboses rares atypiques ont été observées de 4 à 28 jours après la vaccination et se caractérisent par :
- Thrombose veineuse et/ou artérielle (quelle que soit la localisation) associée à une diminution des plaquettes (< 150 G/L)
- Thromboses veineuses et/ou artérielles de siège inhabituel (localisation, contexte clinique, éventuellement multi-sites, parfois successives), en particulier thrombose veineuse cérébrale et thrombose veineuse splanchnique.
En cas de diagnostic d’une thrombose atypique chez une personne vaccinée, un traitement anticoagulant par des alternatives à l’héparine doit être privilégié, en raison des réactions similaires connues de l’héparine avec le facteur plaquettaire 4.
Une recherche de la présence dans le plasma d’anticorps anti-FP4 devra être réalisée en parallèle de préférence par un test Elisa adapté.
![]() SYNDROME DE GUILLAIN-BARRÉ (SGB) OU POLYRADICULONÉVRITE :
SYNDROME DE GUILLAIN-BARRÉ (SGB) OU POLYRADICULONÉVRITE :
Le syndrome de Guillain-Barré est une atteinte des nerfs périphériques caractérisée par une faiblesse voire une paralysie progressive, débutant le plus souvent au niveau des jambes et remontant parfois jusqu’à atteindre les muscles de la respiration puis les nerfs de la tête et du cou.
Toute personne vaccinée doit consulter immédiatement un médecin si elle développe des signes et des symptômes évocateurs de SGB, tels qu'une vision double ou difficulté à bouger les yeux, une difficulté à avaler, à parler ou à mâcher, des problèmes de coordination et d’instabilité, une difficulté à marcher, des sensations de picotements dans les mains et les pieds, une faiblesse dans les membres, la poitrine ou le visage, des problèmes de contrôle de la vessie et de la fonction intestinale.
POUR L'HISTOIRE : LES PREMIERS VACCINS
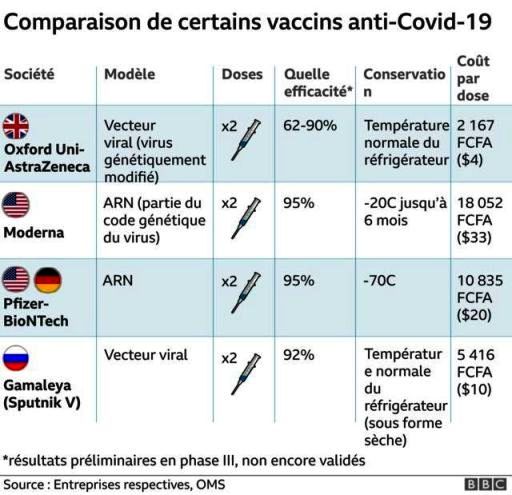
1/ VACCIN ASTRA-ZENECA (ou VAXZEVRIA®) :
Ce vaccin est autorisé dans les pays membres de l'Union européenne depuis le 29 janvier 2021.
- Le 2 février 2021, en raison de données insuffisantes chez les personnes âgées, la Haute Autorité de santé a recommandé de restreindre son usage aux personnes âgées de moins de 65 ans.
- Mise à jour du 11 juin 2021 : Le comité de sécurité de l'EMA a conclu que les personnes qui ont déjà eu le SYNDROME DE FUITE CAPILLAIRE ne doivent pas être vaccinées avec Vaxzevria (Vaccine AstraZeneca). c'est une maladie très rare et grave qui provoque une fuite de liquide des capillaires, entraînant un gonflement principalement dans les bras et les jambes, une pression artérielle basse, un épaississement du sang et de faibles taux sanguins d'albumine.
- Mise à jour du 26/03/2021 : L'Agence du médicament (ANSM) a confirmé l'existence d'un risque "rare" de THROMBOSE atypique associé au vaccin AstraZeneca, après la survenue de nouveaux cas en France, dont deux décès, tout en soulignant que la balance bénéfice/risque restait favorable.
![]() La Haute Autorité de Santé en France a décidé le 19 mars 2021 de restreindre l'utilisation du vaccin Astra-Zeneca aux personnes de plus de 55 ans.
La Haute Autorité de Santé en France a décidé le 19 mars 2021 de restreindre l'utilisation du vaccin Astra-Zeneca aux personnes de plus de 55 ans.
Pour en savoir plus : Vaccin AstraZeneca et accidents thromboemboliques
- AstraZeneca a annoncé, jeudi 25 mars, que son vaccin contre le Covid-19 était efficace à 76% pour prévenir les cas symptomatiques (85% chez les 65 ans et plus).
- La possibilité de vaccins mixtes (recevoir une première dose d'AstraZeneca et une seconde de Pfizer ou de Moderna) est encore à l'étude.
Il s'agit de flacons multidoses contenant 8 doses ou 10 doses de 0,5 ml par flacon.
Une dose (0,5 ml) contient : Adénovirus de chimpanzé codant pour la glycoprotéine Spike du SARS-CoV-2.
Ce produit contient des organismes génétiquement modifiés.
Liste des excipients :
L-histidine, Chlorhydrate de L-histidine monohydraté, Chlorure de magnésium hexahydraté, Polysorbate 80 (E 433), Éthanol, Saccharose, Chlorure de sodium, Édétate disodique dihydraté, Eau pour préparations injectables
Posologie :
Deux doses distinctes de 0,5 ml chacune. La seconde dose doit être administrée entre 4 et 12 semaines (28 à 84 jours) après la première dose.
Mode d’administration :
Par voie intramusculaire (IM), de préférence dans le muscle deltoïde de la partie supérieure du bras.
Effets indésirables :
- Très fréquents : Sensibilité au site d’injection Douleur au site d’injection Chaleur au site d’injection Prurit au site d’injection Ecchymoses au site d'injection Fatigue Malaise État fébrile Frissons. Céphalées, nausées. Myalgies Arthralgies Myalgies Arthralgies
- Fréquents : Gonflement au site d’injection, Érythème au site d’injection, Fièvre
- Peu fréquents : Étourdissements, Somnolence, Diminution de l’appétit, Lymphadénopathie
2/ VACCIN PFIZER-BIONTECH COVID-19 (ou COMIRNATY®)
Comirnaty dispersion à diluer pour solution injectable est un Vaccin à ARNm (à nucléoside modifié) contre la COVID-19
Le médicament est fourni dans un flacon multidose et doit être dilué avant utilisation.
Un flacon contient 6 doses de 0,3 mL après dilution par 1,8 mL de solution injectable de chlorure de sodium 0,9%.
1 dose (0,3 mL) contient 30 microgrammes de vaccin à ARNm contre la COVID-19 (encapsulé dans des nanoparticules lipidiques).
L’ARN messager (ARNm) simple brin à coiffe en 5’ est produit à l’aide d’une transcription in vitro sans cellule à partir des matrices d’ADN correspondantes et codant pour la protéine Spike (S) virale du SARS-CoV-2.
Posologie et administration :
Personnes âgées de 16 ans et plus : Comirnaty doit être administré par voie intramusculaire, après dilution, selon un schéma de vaccination en 2 doses (de 0,3 mL chacune). Il est recommandé d’administrer la seconde dose 3 semaines après la première dose.
Population gériatrique : Aucun ajustement posologique n’est nécessaire chez les personnes âgées de ≥ 65 ans.
Contre-indications :
Hypersensibilité à la substance active ou à l’un des excipients.
Effets indésirables :
Les effets indésirables les plus fréquents étaient une douleur au site d’injection (> 80 %), une fatigue (> 60 %), des céphalées (> 50 %), des myalgies et des frissons (> 30 %), des arthralgies (> 20 %), une fièvre et un gonflement au site d’injection (> 10 %). Ces effets ont été généralement d’intensité légère ou modérée et se sont résolus en quelques jours après la vaccination. Une moindre fréquence de la réactogénicité a été observée chez les sujets les plus âgés.
Précautions particulières de conservation :
À conserver au congélateur entre -90 °C et -60 °C.
À conserver dans l’emballage d’origine, à l’abri de la lumière.
3/ VACCIN MODERNA (ou SPIKEVAX®):
Vaccin à ARNm (à nucléoside modifié) contre la COVID-19
Ce vaccin a été autorisé par l'agence européenne des médicaments (EMA) le 6 janvier 2021.
![]() Juillet 2021 : Dépôt d'un dossier de demande d'autorisation auprès de l'Agence européenne des médicaments pour les adolescents âgés de 12 à 17 ans.
Juillet 2021 : Dépôt d'un dossier de demande d'autorisation auprès de l'Agence européenne des médicaments pour les adolescents âgés de 12 à 17 ans.
En cas d'antécédent de covid 19 : attendre 3 à 6 mois avant de vacciner et ne pas administrer plus d'une dose chez les personnes non immunodéprimées.
Préférer un vaccin à ARNm à partir de l'âge de 55 ans.
Il s’agit d’un flacon multidose, qui contient 10 doses de 0,5 ml. Une dose (0,5 ml) contient 100 microgrammes d’ARN messager (ARNm).
À conserver congelé entre -25 et -15 °C
Décongeler avant utilisation : 2h30 au réfrigérateur puis 1 heure à température ambiante
Posologie :
En 2 doses (0,5 ml chacune). Il est recommandé d’administrer la seconde dose 28 jours après la première.
Mode d’administration :
Le vaccin doit être administré par voie intramusculaire. Le site privilégié est le muscle deltoïde de la partie supérieure du bras.
Effets indésirables :
Très fréquent (pouvant toucher plus de 1 personne sur 10) :
- gonflement dans l’aisselle - maux de tête - nausées - vomissements - douleur musculaire, douleur articulaire et raideur - douleur ou gonflement au site d’injection - fatigue importante - frissons – fièvre
Fréquent (peut toucher jusqu’à 1 personne sur 10) :
- éruption cutanée - éruption cutanée, rougeur ou urticaire au site d’injection
Peu fréquent (pouvant toucher plus de 1 personne sur 100) :
- démangeaisons au site d’injection
Rare (pouvant toucher plus de 1 personne sur 1000) :
- paralysie soudaine et temporaire des muscles d’un côté du visage entrainant un affaissement - gonflement du visage (le gonflement du visage survient chez les patients qui ont reçu des injections cosmétiques du visage).
Fréquence indéterminée :
- réactions allergiques sévères (anaphylaxie) - hypersensibilité
4/ SPOUTNIK V OU GAM-COVID-VAC.
Vaccin à vecteur viral non réplicatif (Adénovirus), combiné pour la prévention de l'infection par le virus SARS-CoV-2
Le vaccin Sputnik V, du laboratoire russe Gamaleya, utilise la protéine S (ou protéine de spicule) complète du SARS-CoV-2, dont le gène est inséré dans le génome d'un adénovirus humain non réplicatif de type 26 ou de type 5.
Chaque dose de vaccin Sputnik V contient 10¹¹ particules virales recombinantes (de l'adénovirus 26 ou bien de l'adénovirus 5) exprimant la protéine S.
Présentation :
Solution pour injection intramusculaire pour 2 doses
Composant I : 0,5 ml/dose + composant II : 0,5 ml/dose
Stockage :
6 mois - préparation congelée : dans un endroit sombre, à une température ne dépassant pas moins 18 degrés.
2 mois - préparation liquide : dans un endroit sombre à une température de 2 à 8 degrés (ne pas congeler).
Posologie :
Deux doses par voie intramusculaire : J0 et J21.
Le schéma vaccinal comporte deux doses administrées par voie intramusculaire à 21 jours d'intervalle. Une dose contenant l'adénovirus recombinant rAd26-S est administrée à J0 et une dose contenant l'adénovirus recombinant rAd5-S est administrée à J21 jours.
Effets indésirables :
D’après les études publiées, les effets indésirables les plus fréquents dans le groupe vacciné étaient un syndrome pseudo-grippal, hyperthermie, douleur articulaire, céphalée et une réaction locale (5,4 % contre 1,2 % dans le groupe placebo).
Références :
5/ VACCIN SINOPHARM COVID-19 (BIBP-CorV )
Sinopharm/China National Pharmaceutical Group
Vaccin entier inactivé approuvé par l'OMS. En attendant des études :
- l’OMS recommande d’utiliser le vaccin BIBP contre la COVID-19 chez les femmes enceintes lorsque les avantages de la vaccination pour la femme concernée l’emportent sur les risques potentiels. Théoriquement il n'y a pas de risque.
- Il n'est pas recommandé pour les moins de 18 ans.
Adjuvant :
Hydroxyde d'aluminium, le tris- (hydroxyméthyl) -aminométhane, le chlorure de sodium, le saccharose, le chlorure de magnésium hexahydraté, l'EDTA disodique dihydraté, le polysorbate 80, l'éthanol et l'eau.
Forme et présentation :
Seringue pré remplie de 0,5 mL.
Conservation :
Entre 2 et 8° C
Posologie :
Deux doses en IM à 3 semaines d'intervalle : J0, J21
Effets indésirables :
L'effet indésirable le plus fréquent était la douleur au point d'injection, suivie de la fièvre, qui était légère et de courte durée ; aucun effet indésirable grave n'a été observé d’après le laboratoire.
6/ CORONAVAC© du laboratoire chinoix SINOVAC :
Vaccin anti-covid 19 entier inactivé avec adjuvant. Il utilise une technologique classique.
Vaccin approuvé par l'OMS. En attendant des études :
- l’OMS recommande d’utiliser le vaccin BIBP contre la COVID-19 chez les femmes enceintes lorsque les avantages de la vaccination pour la femme concernée l’emportent sur les risques potentiels. Théoriquement il n'y a pas de risque.
- Il n'est pas recommandé pour les moins de 18 ans.
Adjuvant :
Hydroxyde d'aluminium
Posologie :
Deux doses en injection IM à 2 semaines d'intervalle : J0 et J14 (entre 2 à 4 semaines).
Efficacité :
Les données communiquées au Brésil (essai clinique phase 3) affirment que le vaccin semble sûr, seules quelques personnes présentant des symptômes légers tels que des maux de tête. L’efficacité globale est estimé à 50,38%.
Les chiffres actuels montrent que le taux de protection des vaccins Sinovac dans les deux mois suivant l'administration de deux injections est de 80 à 90%, mais le nombre d'anticorps chez les receveurs diminue avec le temps.

7/ VACCIN JANSSEN (de Janssen-Cilag International, Johnson & Johnson)
Une autorisation de mise sur le marché conditionnelle valide dans toute l’union européenne a été délivrée le 11 mars 2021 par l’EMA.
5 mai 2022 : L'Agence américaine des produits alimentaires et médicamenteux (FDA) a annoncé qu'elle limitait l'utilisation du vaccin du laboratoire pharmaceutique Janssen aux personnes de 18 ans et plus. la FDA et le Centre de contrôle et de prévention des maladies (CDC) ont identifié 60 cas confirmés de syndrome thrombose-thrombocytopénie TTS, dont neuf cas mortels, selon la FDA.
COVID-19 Vaccine Janssen est constitué d’un autre virus (Ad26 de la famille des adénovirus) qui a été modifié de façon à contenir le gène permettant de produire la protéine de spicule («spike») du SARS-CoV-2. Il s’agit d’une protéine située à la surface du virus SARS-CoV-2, dont il a besoin pour pénétrer dans les cellules de l’organisme.
- Flacon (verre) 2,5 mL (5 doses de 0,5 mL). Administré en une seule injection, habituellement dans le muscle du haut du bras.
- La protection par COVID-19 Vaccine Janssen commence environ 14 jours après la vaccination, mais sa durée n’est pas encore connue à l’heure actuelle.
- Les personnes qui présentent une allergie à l’un des composants du vaccin ne doivent pas être vaccinées.
- Population pédiatrique et grossesse : Pas d’études
Adjuvants :
2-hydroxypropyl-β-cyclodextrin (HBCD) • Citric acid monohydrate • Ethanol • Hydrochloric acid • Polysorbate-80 • Sodium chloride • Sodium hydroxide • Trisodium citrate dihydrate • Water for injection
Effets indésirables :
Les effets indésirables les plus couramment observés sont la douleur au site d’injection, les maux de tête, la fatigue, les douleurs musculaires et les nausées. Ils ont touché plus d’une personne sur 10. La toux, des douleurs articulaires, de la fièvre, des frissons et des rougeurs ainsi qu’un gonflement sur le site de l’injection se sont manifestés chez moins d’une personne sur 10. Des éternuements, des tremblements, des maux de gorge, des éruptions cutanées, de la transpiration, une faiblesse musculaire, des douleurs dans les bras et les jambes, des maux de dos, une faiblesse et une sensation générale de malaise se sont manifestés chez moins d’une personne sur 100.
Les effets indésirables rares (qui se sont manifestés chez moins d’une personne sur 1000) sont l’hypersensibilité (allergie) et les éruptions cutanées avec démangeaisons. Des réactions allergiques, y compris un cas d’anaphylaxie (réaction allergique grave), ont été observées chez des personnes recevant le vaccin.
Comme pour tous les vaccins, COVID-19 Vaccine Janssen doit être administré sous surveillance étroite et un traitement médical approprié doit être disponible.
© 2021-2023 Synthèse par efurgences